

选项 | 物质使用 | 解释 |
A |
|
|
B | 高纯硅用于光导纤维、太阳能电池、计算机芯片 | 硅具有半导体性能 |
C | 液晶可作电视显示屏 | 液晶分子可沿电场方向有序排列 |
D |
|
|
 B .
B .  C .
C .  D .
D . 
选项 | 原因 | 结果 |
A | 草酸钙是人体不能吸收的沉淀物 | 卤水豆腐不可与菠菜一起煮 |
B | 三氯化铁具有氧化性 | 三氯化铁可作净水剂 |
C | 聚氯乙烯塑料稳定性比聚乙烯塑料强 | 用聚氯乙烯塑料袋来盛装食品 |
D | 天然气含碳量比液化石油气低 | 燃气灶将天然气改为液化石油气时需增大空气进入量 |
| 选项 | 生产活动 | 化学原理 |
| A | 过氧化钠用于呼吸面具的制造 | 过氧化钠与人呼出的H2O、CO2都能发生反应生成O2 |
| B | 葡萄酒生产时用SO2做食品添加剂 | 二氧化硫具有还原性,且有防腐作用 |
| C | 用氧化铁和铝粉组成的混合物焊接钢轨 | 氧化铁和铝粉剧烈反应放出大量的热,使产物单质铁呈熔融状态 |
| D | 用乙二醇合成涤纶 | 乙二醇与水分子间可形成氢键,可互溶 |
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
2NaHCO3 Na2CO3+CO2↑+H2O
在指定条件下,下列选项所示的物质间转化不能实现的是( )
选项 | 素质教育 | 化学知识或原理 |
A | 音乐:“音乐焰火”创造出火树银花不夜天 | 焰色反应属于化学变化 |
B | 体育:北京冬奥会火炬外壳材料是由高性能树脂与碳纤维融合而成的复合材料 | 该复合材料具有耐高温、耐腐蚀等优良的特性 |
C | 美术:宋代《千里江山图》中的绿色来自孔雀石颜料[主要成分为Cu(OH)2·CuCO3],青色来自蓝铜矿颜料[主要成分为Cu(OH)2·2CuCO3] | 孔雀石、蓝铜矿颜料不易被空气氧化且耐酸、耐碱 |
D | 文学:爆竹声中一岁除,春风送暖入屠苏 | 传统爆炸粉为黑火药,其主要成分为木炭、硫磺、KClO3 |

已知:ⅰ.与酸反应生成
离子,草酸钕晶体[
]的摩尔质量是
;
ⅱ.生成
, 开始沉淀时
, 完全沉淀时
生成
, 开始沉淀时
, 完全沉淀时
下列说法错误的是( )
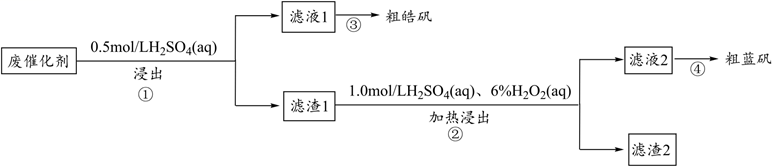 已知:CuS既不溶于稀硫酸,也不与稀硫酸反应。下列说法正确的是( )
已知:CuS既不溶于稀硫酸,也不与稀硫酸反应。下列说法正确的是( )

试剂X可以是;若缺少C装置其后果是(写一条)。
(已知CuCl、CuSCN是难溶于水的白色固体)

请从平衡角度说明红色褪去的可能原因。

①如图蓝色溶液中可能含有的盐有Cu(NO3)2、。
②实验中CuSCN与过量稀HNO3反应生成白色沉淀B的阴离子,同时生成N2、NO和CO2气体。CuSCN与HNO3反应中还原剂与氧化剂的物质的量之比为(已知SCN-中C为+4价)。

已知(NH4)2SO4在350℃分解生成NH3和H2SO4 , 回答下列问题:


①电解时离子交换膜(b)为(填“阴”或“阳”)离子交换膜。
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解,进而提高了Na2FeO4的产率。该反应的离子方程式为。

已知:Ksp(FeAsO4)=5.7×10-21 , H3AsO3的还原性比Fe2+强。
回答下列问题:

已知:65℃时Ksp[Mg(OH)2]= 1.8×10-11 Ksp[Zn(OH)2]=2.0×10-17 Kw=10-13 lg2≈0.3
回答下列有关问题:

已知:碳酸锂的溶解度(g·L-1)见表。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
回答下列问题



当用量倍数为2.0时,水相中的金属阳离子主要含
、(填离子符号).

a.NaCl b. c.
步骤1:准确称取8.884g黄血盐样品加入水中充分溶解,将所得溶液转移至容量瓶并配制成100.00mL溶液。
步骤2:量取25.00mL上述溶液,用酸性
溶液滴定,达到滴定终点时,共消耗
溶液30.50mL。该实验中所发生的反应如下:
①通过计算确定该样品的纯度是(保留3位有效数字)。
②下列操作会使测定结果偏高的是(填字母)。
A.步骤1过程中黄血盐所含亚铁在空气中部分氧化
B.滴定前仰视滴定管读数,滴定后读数正确
C.滴定结束后,滴定管内壁附着液滴
D.滴定前滴定管尖嘴部分有气泡,滴定后尖嘴部分无气泡

已知:①"萃取"时发生反应有:Sc3++3H2A2(有机液)
Sc(HA2)3(有机相)+3H+Fe3++3H2A2(有机液)
Fe(HA2)3+3H+
②常温下,“萃取”前溶液中c(Sc3+)=0.60mol·L-1 , Ksp[Sc(OH)3]=6.0×10-31;请回答下列问题:

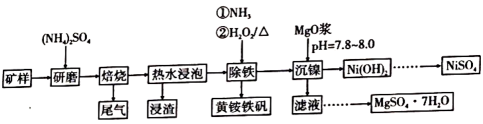
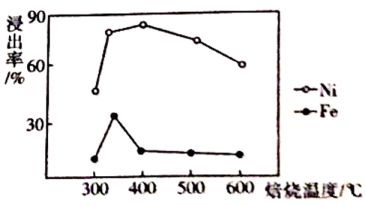
已知:①2[Mg3Si2O5(OH)4]+9(NH4)2SO43(NH4)2Mg2(SO4)3+12NH3↑+4SiO2+10H2O↑;
②2Fe2MgO4+15(NH4)2SO4(NH4)2Mg2(SO4)3+16NH3↑+4(NH4)3Fe(SO4)3+8H2O↑
③常温下,NiSO4易溶于水,NiOOH不溶于水。
沉淀物 | Ni(OH)2 | Fe(OH)3 | 黄铵铁矾 |
开始沉淀时的pH | 7.1 | 2.7 | 1.3 |
沉淀完全(c=1×10-5 mol/L)时的pH | 9.2 | 3.7 | 2.3 |


回答下列问题:

| 开始沉淀的pH | 完全沉淀的pH | |
| | 8.0 | 10.0 |
| | 7.5 | 9.5 |
若将沉铜后的溶液调节至 ,此时溶液中
。
①焙烧氧化的产物有As4O6、Fe3O4 , 该反应的化学方程式为。
②焙烧氧化的缺点为。
③采用电解法除去反应剩余液中有毒物质,CN-在阳极区被去除。在pH=10时,CN-去除效果最佳且能耗最低,原因是。

①工业上利用硫代硫酸盐可浸出金生成Au(S2O3) ,但在富氧条件下浸出率明显降低,原因是。
②常温下,已知H2S-HS--S2-粒子体系随pH变化各组分分布如图-2,δ(H2S)= 。多硫化物浸金的一种原理是:混合体系在通空气条件下氧化时,体系中S2-先被氧化为S,再转化为
。研究发现
可将Au氧化为AuS- , pH=11时
将Au氧化的离子方程式为。
试题篮
0